Vous trouverez ci-dessous le résumé en français du rapport anglais, réalisé par le Laboratoire Chimie Environnement de l’université Aix Marseille et le CNRS : “The purification performance of LaVie system: effect of free chlorine and dissolved oxygen concentration“
Les performances de purification du système LaVie : effet du chlore libre et de la concentration en oxygène dissous

Notes : Nous avons délibérément placé la conclusion sous l’introduction pour permettre rapidement de comprendre les résultats de cette étude sans passer par la partie plus technique.
Introduction et objectifs
Le système LAVIE vise à fournir de l’eau pure et de haute qualité, à la fois agréable à boire et bénéfique pour la santé, tout en offrant une solution d’eau potable pour les pays en développement. Ce système purifie l’eau de réseau contenant du chlore tout en éliminant les bactéries et les virus. Le rapport se concentre sur la démonstration de l’efficacité du système LAVIE pour dégrader les composés organiques par photolyse (c’est-à-dire par l’absorption directe de la lumière) et explore l’efficacité du *chlore libre dans ce processus.
Conclusion
Le système LAVIE démontre clairement son efficacité pour la dégradation des composés organiques en présence de chlore libre et d’oxygène. La photolyse du chlore et la production d’espèces réactives de l’oxygène jouent un rôle crucial dans ce processus, faisant du système LAVIE une méthode innovante pour purifier l’eau du robinet en éliminant les traces de composés pharmaceutiques et autres polluants organiques.
Résumé de l’étude
Matériel et méthodes analytiques
- Produits et réactifs : Utilisation de *Diclofénac (DCF) comme composé de référence, de l’eau de Javel et d’autres produits chimiques spécifiques pour les analyses.
- Préparation des solutions : Solutions de DCF préparées avec de l’eau ultra-pure et mélangées à l’eau du robinet pour obtenir différentes concentrations de DCF et de chlore libre.
- Système de purification LaVie : Équipé de LED UV-A pour une durée d’exposition programmée de 15 minutes.
Méthodes analytiques
- Mesure du chlore libre et de l’oxygène dissous : Utilisation de photomètre et d’électrodes spécifiques pour ces mesures.
- Abattement des composés organiques : Suivi par chromatographie liquide haute performance (HPLC).
Résultats
- Paramètres expérimentaux : Ajustement des concentrations de DCF et de chlore libre pour observer la dégradation significative des composés organiques.
- Effet de la concentration en chlore libre sur la dégradation du DCF :
- Hautes concentrations de DCF : Dégradation du DCF améliorée en présence de chlore libre, avec une relation linéaire observée entre la concentration en chlore et le pourcentage d’élimination du DCF.
- Basses concentrations de DCF : Amélioration de l’élimination du DCF avec l’augmentation de la concentration en chlore libre, confirmant l’implication du chlore dans le processus de dégradation.
- Effet de la concentration en oxygène : Expériences réalisées dans des conditions aérobies et anaérobies montrent que l’élimination de l’oxygène diminue significativement la dégradation du DCF, suggérant l’implication des espèces oxygénées réactives dans le processus.
Références
Une des figures illustrant l’étude
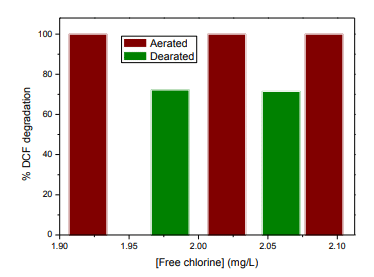
Légende : Dégradation de la DCF en fonction de la concentration en chlore libre dans l’eau du robinet enrichie en eau de Javel après irradiation dans le système LAVIE dans des conditions *aérobies (Aerated) et anaérobies (Dearated), [DCF] = 2,5 mg/L et [chlore libre] environ 2 mg/L.
Questions / Réponses
*Qu'est ce que le chlore libre ?
Le chlore libre désigne le chlore disponible dans l’eau sous forme de chlore actif, capable de désinfecter et de détruire les micro-organismes. Il existe principalement sous deux formes :
- Acide hypochloreux (HOCl) : C’est la forme la plus efficace pour la désinfection car elle pénètre facilement les parois des cellules des micro-organismes.
- Ion hypochlorite (OCl⁻) : C’est une forme moins efficace de chlore libre en raison de sa charge ionique, qui limite sa capacité à pénétrer les cellules.
Le chlore libre est souvent utilisé dans le traitement de l’eau potable pour tuer les bactéries, les virus et autres pathogènes, ainsi que pour oxyder les contaminants chimiques. Sa concentration est mesurée pour garantir l’efficacité de la désinfection tout en minimisant la formation de sous-produits indésirables tels que les trihalométhanes (THM).
Quelle relation entre l’eau de javel et le chlore libre ?
La javel et le chlore libre sont liés mais ne sont pas exactement la même chose.
Eau de Javel :
- L’eau de Javel est une solution aqueuse contenant de l’hypochlorite de sodium (NaClO). C’est un produit chimique utilisé principalement comme désinfectant et agent de blanchiment.
- Lorsqu’elle est dissoute dans l’eau, l’hypochlorite de sodium se dissocie en ions hypochlorite (OCl⁻) et en acide hypochloreux (HOCl), ce qui contribue à son action désinfectante.
Chlore libre :
- Le chlore libre dans l’eau se réfère aux formes actives de chlore, principalement l’acide hypochloreux (HOCl) et l’ion hypochlorite (OCl⁻).
- C’est le chlore libre qui est responsable de l’effet désinfectant dans l’eau traitée. Le terme “chlore libre” est utilisé pour mesurer la quantité de chlore disponible pour la désinfection dans l’eau potable ou de piscine.
Relation entre les deux :
- Lorsqu’on ajoute de l’eau de Javel à l’eau, elle libère du chlore libre sous forme d’acide hypochloreux (HOCl) et d’ions hypochlorite (OCl⁻).
- En ce sens, la javel est une source de chlore libre lorsqu’elle est ajoutée à l’eau.
Résumé :
– Eau de Javel = source de chlore libre (hypochlorite de sodium en solution).
– Chlore libre = formes actives (HOCl et OCl⁻) de chlore dans l’eau, dérivées de l’eau de Javel ou d’autres sources de chlore.
Pourquoi le diclofénac (DCF), considéré toxique, a-t-il été inclus dans cette expérience ?
- Toxicité : Le diclofénac, un anti-inflammatoire non stéroïdien (AINS) couramment utilisé pour traiter la douleur et l’inflammation, est souvent détecté dans les eaux de surface et les eaux usées en raison de son utilisation répandue et de son excrétion par l’organisme. Même à de faibles concentrations, il peut avoir des effets toxiques sur la vie aquatique, notamment sur les poissons et les invertébrés aquatiques.
- Présence dans l’eau du robinet : Bien que généralement à des concentrations très faibles, le diclofénac peut être trouvé dans l’eau du robinet, résultant de l’incapacité des stations d’épuration à éliminer complètement les résidus pharmaceutiques.
- Inclusion dans l’expérience : Le diclofénac a été utilisé dans cette étude comme composé de référence pour évaluer l’efficacité du système LAVIE à dégrader les contaminants organiques présents dans l’eau du robinet. Cela permet de démontrer la capacité du système à éliminer des traces de produits pharmaceutiques, améliorant ainsi la qualité de l’eau potable.
Pourquoi les expériences ont-elles été réalisées en conditions aérobie (aerated) et anaérobie (dearated) ?
Les expériences ont été menées en conditions aérobies et anaérobies pour évaluer l’impact de l’oxygène dissous sur l’efficacité du système de purification LAVIE.
- Aérobie (aerated) : L’eau contient de l’oxygène dissous, favorisant la formation d’espèces réactives de l’oxygène (ERO) comme les radicaux hydroxyles, qui dégradent efficacement les contaminants.
- Anaérobie (dearated) : L’eau est dépourvue d’oxygène dissous, ce qui limite la formation des ERO et réduit l’efficacité de la dégradation des contaminants.
Conclusion : La présence d’oxygène dissous améliore significativement la dégradation du diclofénac par le système LaVie, démontrant l’importance des conditions aérobies (c’est à dire avec le taux d’oxygène normal que l’on trouve dans l’eau du robinet) pour une purification optimale.